GIF wstrzymuje w obrocie kolejne leki: Levosimendan Kabi, Clotidal MAX i Egoropal
- Publikacja:
- 2023-10-12 17:36
- Aktualizacja:
- 2025-06-03 14:20
W ostatnich dniach Główny Inspektorat Farmaceutyczny opublikował kilka decyzji wstrzymujących w obrocie leki, które niedawno wprowadzono po raz pierwszy do sprzedaży. 12 października 2023 r. wydano kolejne decyzje wstrzymujące dla leków Levosimendan Kabi, Clotidal MAX i Egoropal. Dlaczego wstrzymano obrót tymi produktami leczniczymi?
Artykuł rekomendowany przez:

Levosimendan Kabi – co to za lek i kiedy się go stosuje?
Substancją czynną zastosowaną w leku Levosimendan Kabi jest lewozymendan. Lek ma postać koncentratu do sporządzania roztworu do infuzji i przeznaczony jest do stosowania wyłącznie w szpitalach.
Lek Levosimendan Kabi stosuje się w krótkotrwałym leczeniu ostrej, zdekompensowanej, ciężkiej przewlekłej niewydolności serca (ADHF, ang. acutely decompensated severe chronic heart failure), gdy konwencjonalne leczenie jest niewystarczające lub jeśli zastosowanie leków o działaniu inotropowym dodatnim jest właściwe.
Dlaczego wstrzymano obrót lekiem Levosimendan Kabi?
9 października 2023 r. do GIF wpłynął protokół cząstkowy badania przeprowadzonego przez Narodowy Instytut Leków (NIL). W protokole wskazano, że przebadana próbka leki nie spełnia wymagań jakościowych dla parametru zanieczyszczenia cząstkami widocznymi okiem nieuzbrojonym. Istnieje zatem uzasadnione podejrzenie, że produkt nie będzie odpowiadał ustalonym dla niego wymaganiom.
Zgodnie z decyzją numer 10/2023 z dnia 12 października 2023 r. wstrzymano na terenie całego kraju obrót produktem leczniczym o nazwie Levosimendan Kabi (Levosimendanum) koncentrat do sporządzania roztworu do infuzji 2,5 mg/ml,
- 1 fiolka po 5 ml GTIN 05909991485894
- 4 fiolki po 5 ml GTIN 05909991485917
- 10 fiolek po 5 ml GTIN 05909991485900
Podmiotem odpowiedzialnym jest Fresenius Kabi Polska Sp. z o.o. z siedzibą w Warszawie.
Clotidal MAX – wskazania do stosowania
Substancją czynną zastosowaną w leku Clotidal MAX jest klotrimazol – lek przeciwgrzybiczy o szerokim zakresie działania, pochodna imidazolu. Lek wykazuje skuteczność wobec dermatofitów, drożdżaków i pleśni. Ma postać tabletki dopochwowej.
Clotidal MAX wskazany jest w leczeniu zakażeń pochwy i sromu (żeńskich zewnętrznych narządów płciowych) wywołanych przez grzyby wrażliwe na klotrimazol (zazwyczaj Candida). Clotidal MAX może być stosowany u osób dorosłych i młodzieży od 16. roku życia. W aptekach lek dostępny jest bez recepty.
Co było przyczyną wstrzymania obrotu lekiem Clotidal MAX?
Jak możemy przeczytać w dokumencie, przyczyną wstrzymania w obrocie był niekorzystny wynik badania przeprowadzonego przez NIL:
„ (…) produkt ten nie spełnia przewidzianych dla niego wymagań jakościowych z uwagi na negatywny wynik badania w zakresie parametru Wygląd”
Według danych serwisu KtoMaLek.pl tylko w ciągu ostatnich 30 dni sprzedano ponad 20 000 opakowań leku Clotidal Max. Najwięcej opakowań leku wykupiono na terenie Warszawy (ponad 1500), a także Krakowa, Wrocławia, Łodzi i Poznania.
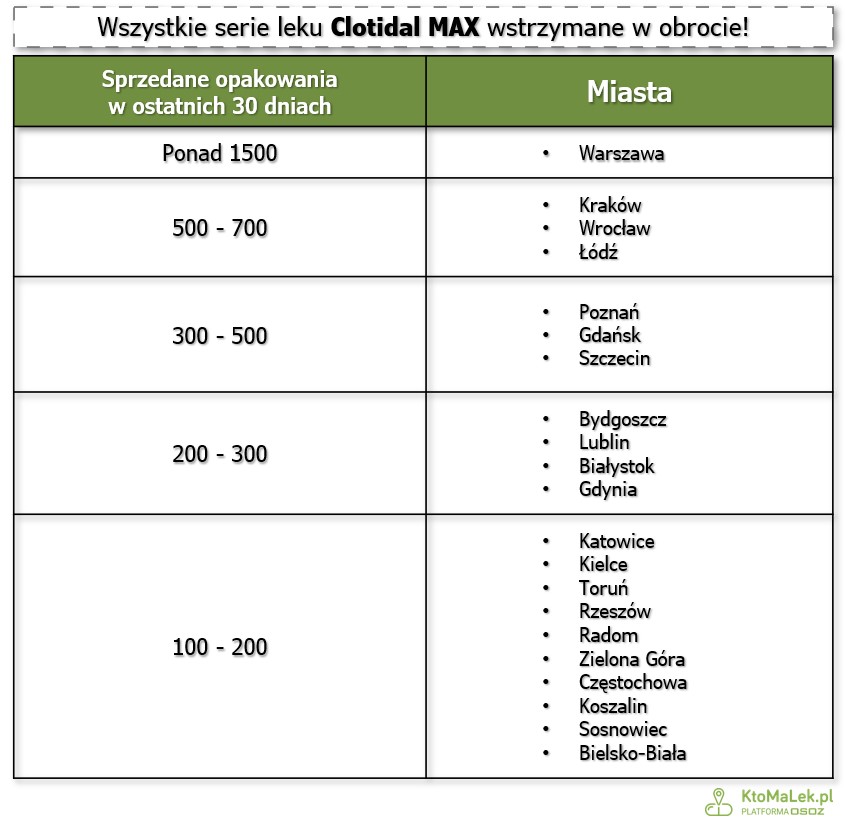
Zgodnie z decyzją numer 12/2023 z dnia 12 października 2023 r. wstrzymano obrót produktem leczniczym o nazwie Clotidal MAX (Clotrimazolum), tabletka dopochwowa, 500 mg
- opakowanie 1 tabletka, GTIN 05909991460907
Podmiotem odpowiedzialnym jest US Pharmacia Sp. z o.o. z siedzibą we Wrocławiu.
Kiedy stosuje się lek Egoropal?
Substacją czynną zastosowaną w leku Egoropal jest paliperydon - lek przeciwpsychotyczny, pochodna benzizoksazolu. Lek ma postać zawiesiny do wstrzykiwań o przedłużonym uwalnianiu w ampułko-strzykawce.
Lek Egoropal wskazany jest w leczeniu podtrzymującym w schizofrenii u dorosłych pacjentów, u których udało się uzyskać stabilizację choroby za pomocą paliperydonu lub rysperydonu. Lek stosuje się też u wybranych pacjenów, u których wystąpiła odpowiedź na leczenie doustne paliperydonem lub rysperydonem.
Dlaczego GIF wstrzymał obrót lekiem Egoropal?
Podobnie jak opisane wcześniej leki, również Egoropal poddany został badaniu przez Narodowy Instytut Leków. Z protokołu przeprowadzonych badań wynika, że lek nie spełnia wymagań jakościowych – uzyskano negatywny wynik badania w zakresie parametru analiza wielkości cząstek.
Zgodnie z decyzją nr 11/2023 z dnia 12 października 2023 r. wstrzymano na terenie całego kraju obrót lekiem Egoropal (Paliperidonum), zawiesina do wstrzykiwań o przedłużonym uwalnianiu w ampułkostrzykawce, 75 mg, GTIN 05995327188706.
Podmiotem odpowiedzialnym jest Egis Pharmaceuticals PLC z siedzibą w Budapeszcie, Węgry.
Źródła:
- https://rdg.ezdrowie.gov.pl/Decision/Decision?id=4408
- https://rdg.ezdrowie.gov.pl/Decision/Decision?id=4409
- https://rdg.ezdrowie.gov.pl/Decision/Decision?id=4410
- https://rejestrymedyczne.ezdrowie.gov.pl/api/rpl/medicinal-products/43865/characteristic
- https://rejestrymedyczne.ezdrowie.gov.pl/api/rpl/medicinal-products/43650/characteristic
- https://rejestrymedyczne.ezdrowie.gov.pl/api/rpl/medicinal-products/43495/characteristic
Autor
Redakcja ktomalek.pl - Zespół redakcyjny KtoMaLek.pl tworzą doświadczeni farmaceuci, którzy specjalizują się w różnych obszarach tematyki zdrowotnej. Doświadczenie zdobyte w zawodzie oraz wiedza uzyskana podczas studiów farmaceutycznych, pozwalają na tworzenie merytorycznych treści zgodnych z EBM (and. Evidence-based Medicine), opartych na rzetelnych źródłach — aktualnych badaniach naukowych, branżowych podręcznikach i książkach. Za praktyką podążają również pasja i niesłabnąca chęć do poszerzania wiedzy oraz dzielenia się nią z pacjentami. Dzięki temu użytkownicy otrzymują dostęp do ciekawych i angażujących materiałów edukacyjnych.


















