GIF wycofuje 5 serii leku Tirosint Sol
- Publikacja:
- 2023-02-22 09:27
- Aktualizacja:
- 2025-06-03 14:20
21 lutego 2023 r. na łamach strony Głównego Inspektoratu Farmaceutycznego pojawił się komunikat na temat wycofania z obrotu 5 serii leku stosowanego m.in. w niedoczynności tarczycy. Mowa o leku Tirosint Sol, dostępnego w postaci roztworu doustnego. Dlaczego GIF zdecydował o wycofaniu tego leku? Sprawdź, których serii preparatu dotyczy ta decyzja!
Artykuł rekomendowany przez:
Tirosint Sol – co to za lek i kiedy się go stosuje?
Substancją czynną leku Tirosint Sol jest lewotyroksyna – analog tyroksyny, jeden z hormonów wydzielanych przez gruczoł tarczowy. Tirosint Sol wskazany jest w przypadku:
- leczenia łagodnego wola w stanie eutyreozy;
- niedoczynności tarczycy w ramach terapii substytucyjnej hormonu tarczycy;
- leczenia supresyjnego w złośliwym nowotworze tarczycy;
- terapii wspomagającej w leczeniu nadczynności tarczycy lekami przeciwtarczycowymi;
- testu supresyjnego tarczycy.
Tirosint Sol ma postać roztworu doustnego, dostępnego w pojemnikach jednodawkowych. Pojemniki jednodawkowe opatrzone są kolorową etykietą, której barwa zależna jest od mocy dawki leku. Produkt wydawany jest wyłącznie na receptę lekarską.
Dlaczego wycofano z obrotu 5 serii Tirosint Sol?
Do Głównego Inspektoratu Farmaceutycznego wpłynęły 2 komunikaty Rapid Alert. Pierwszy z nich przesłany został przez FDA (U.S. Food and Drug Administration), w którym poinformowano o prewencyjnym wycofaniu przez firmę IBSA Pharma Inc. na rynku amerykańskim 5 serii leku Tirosint Sol. Drugi komunikat przesłał hiszpańska agencja Spanish Agency of Medicines And Medical Devices, informując o wycofaniu z rynku hiszpańskiego 5 serii produktu leczniczego, który występuje pod nastą Solsint. W obu przypadkach powodem wycofania były nieprawidłowości w zakresie zawartości substancji czynnej - lewotyroksyny.
W toku działań wyjaśniających potwierdzono, że w przypadku 5 serii leku dostępnych na rynku polskim zawartość substancji czynnej jest obniżona, co rodzi ryzyko zmniejszonej skuteczności działania leku i zagraża zdrowiu pacjentów.
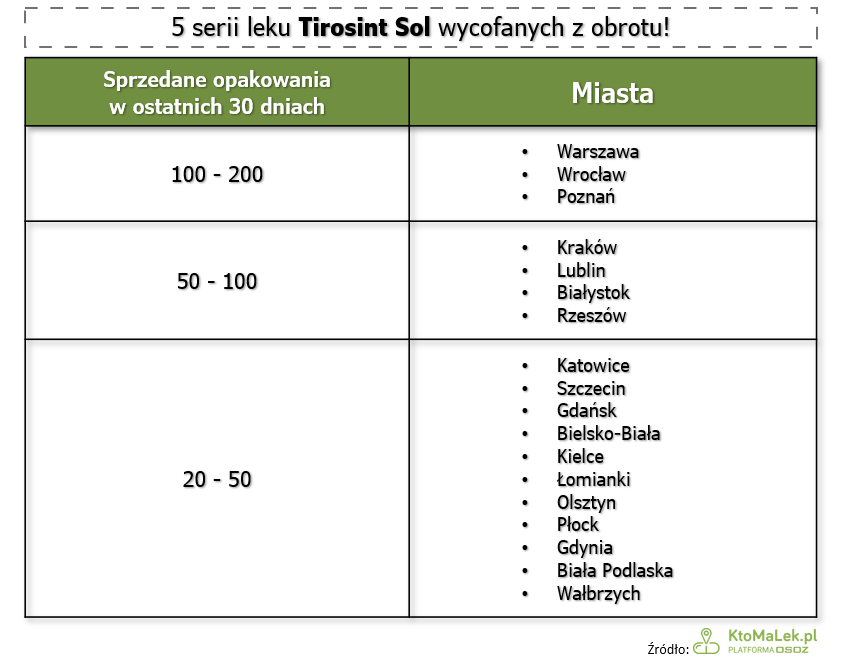
Według danych serwisu KtoMaLek.pl ciągu ostanich 30 dni sprzedano ponad 2700 opakowań wadliwych serii leku. Najwięcej wykupiono w aptekach na terenie Warszawy, Wrocławia i Poznania.
Zgodnie z decyzją numer 6/2023 wycofano z obrotu na terenie całego kraju produkty lecznicze:
TIROSINT SOL (Levothyroxinum natricum), 13 mcg, roztwór doustny w pojemniku jednodawkowym
- numer serii 220551, data ważności: 30.11.2023
TIROSINT SOL (Levothyroxinum natricum), 175 mcg, roztwór doustny w pojemniku jednodawkowym
- numer serii: 220554 data ważności: 30.11.2023
TIROSINT SOL (Levothyroxinum natricum), 100 mcg, roztwór doustny w pojemniku jednodawkowym
- numer serii: 220557, data ważności: 30.11.2023
TIROSINT SOL (Levothyroxinum natricum), 25 mcg, roztwór doustny w pojemniku jednodawkowym
- numer serii 220657, data ważności: 31.12.2023
TIROSINT SOL (Levothyroxinum natricum), 125 mcg, roztwór doustny w pojemniku jednodawkowym
- numer serii: 220753, data ważności: 31.01.2024
Źródła:
- https://www.ibsapoland.pl/dam/jcr:c44ef999-7a48-4158-94e6-c5609582764e/TirosintSOL%20-%20ChPL.pdf
- https://rdg.ezdrowie.gov.pl/Decision/Decision?id=4334
- https://rdg.ezdrowie.gov.pl/Decision/Decision?id=4335
- https://rdg.ezdrowie.gov.pl/Decision/Decision?id=4336
- https://rdg.ezdrowie.gov.pl/Decision/Decision?id=4337
- https://rdg.ezdrowie.gov.pl/Decision/Decision?id=4338
Autor
Redakcja ktomalek.pl - Zespół redakcyjny KtoMaLek.pl tworzą doświadczeni farmaceuci, którzy specjalizują się w różnych obszarach tematyki zdrowotnej. Doświadczenie zdobyte w zawodzie oraz wiedza uzyskana podczas studiów farmaceutycznych, pozwalają na tworzenie merytorycznych treści zgodnych z EBM (and. Evidence-based Medicine), opartych na rzetelnych źródłach — aktualnych badaniach naukowych, branżowych podręcznikach i książkach. Za praktyką podążają również pasja i niesłabnąca chęć do poszerzania wiedzy oraz dzielenia się nią z pacjentami. Dzięki temu użytkownicy otrzymują dostęp do ciekawych i angażujących materiałów edukacyjnych.


















